Il biofilm, ovvero l’insieme complesso dei microrganismi che popolano la nostra bocca e che aderisce a denti e gengive, se si accumula sulle gengive può compromettere l’intero impianto. Nuovi studi stanno mettendo a punto materiali che possano resistere all’attacco batterico.
Perimplantite: l’incidenza del biofilm
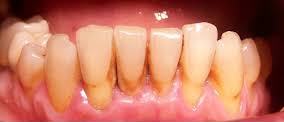
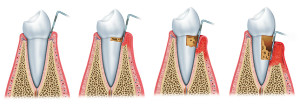
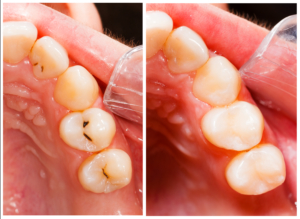 Gengiviti, carie, parodontite e perimplantite sono causate da una patina di batteri che aderisce alle superfici dei denti e attacca smalto e tessuti causandone l’infiammazione e l’infezione.
Gengiviti, carie, parodontite e perimplantite sono causate da una patina di batteri che aderisce alle superfici dei denti e attacca smalto e tessuti causandone l’infiammazione e l’infezione.
Gli impianti dentali non sono esclusi da questa problematicità, il contatto delle protesi dentali con il biofilm ha una forte incidenza sulla possibilità di sviluppare una perimplantite.
Anche un’infezione su denti adiacenti all’impianto potrebbe essere dannosa per la sopravvivenza dell’impianto stesso, motivo per cui la ricerca scientifica si sta orientando allo sviluppo di materiali che possano inibire l’adesione della carica batterica sulla protesi.
Proteggere gli impianti dentali grazie a nuovi materiali
La ricerca in ambito odontoiatrico ha dimostrato in questi anni che la microsuperficie dell’impianto influisce sulla capacità del biofilm di aderire all’area implantare.
Per tale ragione, i ricercatori stanno mettendo a punto un nuovo materiale che abbia delle proprietà antibatteriche e sia bioceramica inerte.
Si tratta di un biomateriale nanocomposito ceramico (Al2O3/Ce-TZP) che ha tutte le proprietà necessarie per l’osteointegrazione, ma allo stesso tempo garantisce un ridotto accumulo di batteri in prossimità dell’impianto.
Studio sperimentale per limitare il rischio perimplantite
Sulla rivista scientifica Dental Materials di giugno 2019 è stata pubblicata una ricerca che mette a confronto l’aderenza del biofilm su diversi biomateriali ceramici utilizzati nell’ambito dell’implantologia.
In particolare è stata analizzata l’adesione dei seguenti batteri standard, molto comuni nel cavo orale:
- Streptococcus oralis;
- Veillonella parvula;
- Actinomyces naeslundii;
- Fusobacterium nucleatum;
- Aggregatibacter actinomycetemcomitans;
- Porphyromonas gingivalis.
I biomateriali messi a confronto con le colonie di batteri sopraelencate erano:
- idrossiapatite di calcio (HA);
- nanocomposito sterile Al2O3/Ce-TZP sabbiato (materiale A1);
- nanocomposito sterile Al2O3/Ce-TZP sabbiato e rivestito con un tipo di materiale vetroso antimicrobico (materiali A2);
- nanocomposito sterile Al2O3/Ce-TZP sabbiato e rivestito con un altro tipo di materiale vetroso antimicrobico (materiale A3).
Risultati
 Dall’analisi è emerso che l’adesione dei batteri era ridotta nei gruppi in cui erano presenti i materiali vetrosi antimicrobici A2 e A3.
Dall’analisi è emerso che l’adesione dei batteri era ridotta nei gruppi in cui erano presenti i materiali vetrosi antimicrobici A2 e A3.
In particolare il materiale ceramico A3, con biocida di vetro arricchito ZnO, ha un significativo effetto antibatterico e può rappresentare un valido aiuto nella progettazione e realizzazione di impianti dentali da utilizzare nell’ambito dell’implantologia.
Questi studi dovranno essere confermati da altri studi, non solo in vitro, ma rappresentano un buon inizio per trovare una soluzione importante nel contrasto alla perimplantite.